中國附醫、長聖合作 細胞療法申請獲准
五月 18, 2019衛生福利部正式開放「實體癌第四期」之自體免疫細胞(DC)治療,長聖國際生技公司與中國醫藥大學附設醫院率先以細胞治療八大實體癌症的第四期病患
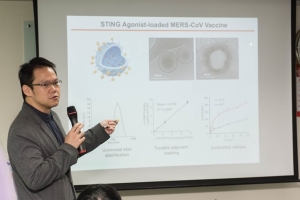
奈米級的模仿!冠狀病毒疫苗可望破解MERS
五月 14, 2019令各國聞之色變、有「新SARS」之稱的「中東呼吸道症候群」(Middle East Respiratory Syndrome, MERS),因其病毒變異快速,至今沒有任何有效的疫苗或藥物。如今,結合奈米科技及冠狀病毒研究,可望獲得解方!
中樞神經再生露曙光 人工合成八醣體可修復脊髓神經元
五月 14, 2019中樞神經受損造成的傷害往往難以修復,如車禍或工害造成的癱瘓。中央研究院基因體研究中心洪上程主任與日本名古屋大學醫學院門松健治院長的最新跨國研究發現,人工合成的「硫酸乙醯肝素(HS) 」八醣體可讓受損的中樞神經元成功啟動修補機制。論文已於5月7日刊登於國際期刊《自然-化學生物學》(Nature Chemical Biology)。
2019.07.25 l 藥品小批量生產趨勢研討會
七月 25, 2019台灣生技產業環境已逐漸完善,製藥產業也全面性的提升,已有多家藥廠與國際接軌成果豐碩。但隨著趨愈嚴峻的法規及經貿環境,如何在有限的資源下發展出自我的價值及定位,是我們一直在尋找的機會點。
再生醫療製劑管理條例草案 立院初審無共識
五月 09, 2019行政院在2018年10月已將此草案送至立法院,2019/05/08立法院在社會福利及衛生環境委員會中對再生醫療製劑管理條例草案進行初審,討論過程有許多爭議,也有立委對安全性提出質疑,過程中立委與食藥署官員針對法案到底要用「製劑」還是「製品」就已無法達成共識,且多達一半以上的條文無法達成共識,最終雖通過初審,但多達13個條文後續將再透過朝野黨團協商進行討論。
亞諾法生技鎖定臨床病理市場 推出陰性富集循環腫瘤細胞平台
五月 07, 2019亞諾法生技今天宣布推出 LiquidCell™陰性富集循環腫瘤細胞平台,鎖定臨床病理之應用市場。現今非侵 入性液態活檢檢測標的物包含:循環腫瘤細胞(CTC, circulating tumor cell)、循環腫瘤 DNA(ctDNA, circulating tumor DNA)和胞外泌體(exosome)。
2019.05.19 I 2019細胞治療發展趨勢與臨床應用研討會
四月 29, 2019隨著精準醫療的快速發展,「細胞治療技術」已為全球癌症治療發展趨勢,目前全球已有數百萬患者接受細胞療法,越來越多的臨床證據顯示細胞治療已具有優異治療效果,儼然成為全球高度重視的新興醫療方式。國內衛生福利部實施「特管法」,開放細胞治療技術應用,細胞治療在技術上已具有前瞻性,被視為治療癌症、心血管疾病等重大疾病的新希望。
2019.05.29 l 生物相似藥的法規與開發挑戰研討會
四月 29, 20192019年1月30日,食藥署又重新預告訂定「西藥之專利連結專章施行辦法草案」,而此次則另將生物相似性藥品納入專利連結制度中,明訂「準用」學名藥藥品許可證申請之專利連結相關規定。新草案一出,各界檢討聲浪不斷,然而許多人仍不了解生物相似藥品專利連結後,未來對國內產業及民眾用藥等會產生哪些影響?
2019.06.15 【新藥開發系列】 CRO 主題課程一日營
六月 15, 2019人體臨床試驗是新藥開發最重要的階段,也是整個新藥開發過程資金投入最多的階段,堪稱為新藥開發成敗的關鍵。臨床試驗從策略規劃與試驗設計開始,到完成收案、資料蒐集暨解盲分析,是一個複雜的程序與活動,牽涉相當多專業人員與團隊的分工與合作,必須有良好完善的規畫以及營運執行面的管理。
2019.06.01 【醫材系列】IVD成功策略經驗分享 (一日精修班)
六月 01, 2019課程主題單位:
1. 如何找尋合作夥伴以拓展商機(BD for IVD : Business Development and Commercialization for IVD )
2. 如何充分掌握法規要點,以利取得產品認證(IVD Regulatory Compliance and Device License)
New Articles
Cell Therapy












![衛福部核可之細胞治療執行單位 [持續更新]](https://www.biomaptw.com/media/k2/items/cache/753a82091bdf93df272697e1f26229c2_XL.jpg)